2026-03-24
Circuito cerebral necesario para incorporar nueva información podría estar vinculado a la esquizofrenia
Uno de los síntomas de la esquizofrenia es la dificultad para incorporar información nueva sobre el mundo. Esto puede llevar a que las personas con esquizofrenia tengan problemas para tomar decisiones y, eventualmente, pierdan contacto con la realidad.
Neurólogos del MIT han identificado ahora una mutación genética que parece causar este tipo de dificultad. En un estudio con ratones, los investigadores encontraron que el gen mutado afecta la función de un circuito cerebral responsable de actualizar las creencias basándose en nueva información.
Esta mutación, en un gen llamado grin2a, fue identificada originalmente en un estudio a gran escala de pacientes con esquizofrenia. El nuevo estudio sugiere que los fármacos que actúen sobre este circuito cerebral podrían ayudar con algunos de los deterioros cognitivos observados en personas con esquizofrenia.
"Si este circuito no funciona bien, no se puede integrar la información rápidamente", dice Guoping Feng, profesor James W. y Patricia T. Poitras en Ciencias del Cerebro y Cognitivas en el MIT, miembro del Instituto Broad de Harvard y MIT, y director asociado del Instituto McGovern para la Investigación Cerebral en el MIT. “Estamos bastante seguros de que este circuito es uno de los mecanismos que contribuyen al deterioro cognitivo, que es una parte importante de la patología de la esquizofrenia.”
Feng y Michael Halassa, profesor de psiquiatría y neurociencia y director de investigación traslacional en la Facultad de Medicina de la Universidad de Tufts, son los autores principales del nuevo estudio, que aparece hoy en Nature Neuroscience. Tingting Zhou, científica investigadora en el Instituto McGovern, y Yi-Yun Ho, ex posdoctorado del MIT, son los autores principales del artículo.
Adaptarse a la nueva información
Se sabe que la esquizofrenia tiene un fuerte componente genético. Para la población general, el riesgo de desarrollar la enfermedad es aproximadamente del 1 por ciento, pero este porcentaje sube al 10 por ciento para quienes tienen un padre o hermano con la enfermedad, y al 50 por ciento para personas que tienen un gemelo idéntico con la enfermedad.
Investigadores del Centro Stanley para la Investigación Psiquiátrica en el Instituto Broad han identificado más de 100 variantes genéticas relacionadas con la esquizofrenia, mediante estudios de asociación genómica amplia. Sin embargo, muchas de esas variantes se encuentran en regiones no codificantes del genoma, lo que dificulta entender cómo podrían influir en el desarrollo de la enfermedad.
Más recientemente, investigadores del Centro Stanley utilizaron una estrategia diferente, conocida como secuenciación del exoma completo, para revelar mutaciones genéticas vinculadas a la esquizofrenia. Esta técnica secuencia solo las regiones codificantes de proteínas del genoma, por lo que puede revelar mutaciones localizadas en genes conocidos.
Usando este método en aproximadamente 25,000 secuencias de personas con esquizofrenia y 100,000 secuencias de sujetos de control, los investigadores identificaron 10 genes en los cuales las mutaciones aumentan significativamente el riesgo de desarrollar esquizofrenia.
En el nuevo estudio publicado en Nature Neuroscience, Feng y sus estudiantes crearon un modelo de ratón con una mutación en uno de esos genes, grin2a. Este gen codifica una proteína que forma parte del receptor NMDA — un receptor activado por el neurotransmisor glutamato y que se encuentra a menudo en la superficie de las neuronas.
Zhou investigó si estos ratones mostraban alguno de los comportamientos característicos observados en personas con esquizofrenia. Estos individuos manifiestan muchos síntomas complejos, incluidas psicosis como alucinaciones y delirios (pérdida del contacto con la realidad). Estos síntomas son difíciles de estudiar en ratones, pero es posible estudiar síntomas relacionados como la dificultad para interpretar nueva información sensorial.
Durante las últimas dos décadas, los investigadores de esquizofrenia han hipotetizado que la psicosis puede derivar de una capacidad deteriorada para actualizar creencias basadas en nueva información.
“Nuestro cerebro puede formar una creencia previa de la realidad, y cuando la entrada sensorial llega al cerebro, un cerebro neurotípico puede usar esta nueva información para actualizar la creencia previa. Esto nos permite generar una nueva creencia que se acerca a lo que es la realidad”, dice Zhou. “Lo que sucede en los pacientes con esquizofrenia es que se aferran demasiado a la creencia previa. No usan tanta información actual para actualizar lo que creían antes, por lo que la nueva creencia se desvincula de la realidad.”
Para estudiar esto, Zhou diseñó un experimento que requería que los ratones eligieran entre dos palancas para presionar a fin de obtener una recompensa de comida. Una palanca daba una recompensa baja: los ratones tenían que presionarla seis veces para obtener una gota de leche. La palanca de alta recompensa dispensaba tres gotas por cada presión.
Al comienzo del estudio, todos los ratones aprendieron a preferir la palanca de alta recompensa. Sin embargo, a medida que avanzaba el experimento, el número de presiones necesarias para obtener la alta recompensa aumentaba gradualmente, mientras que no había cambios en la palanca de baja recompensa.
A medida que aumentaba el esfuerzo requerido, los ratones sanos empezaban a cambiar entre las dos palancas. Una vez que tenían que presionar la palanca de alta recompensa unas 18 veces para obtener tres gotas de leche, haciendo el esfuerzo por gota aproximadamente igual para cada palanca, finalmente cambiaban permanentemente a la palanca de baja recompensa. Sin embargo, los ratones con la mutación en grin2a mostraron un patrón de comportamiento diferente. Pasaban más tiempo variando entre las dos palancas y cambiaban a la palanca de baja recompensa mucho más tarde.
“Encontramos que los animales neurotípicos toman decisiones adaptativas en este entorno cambiante”, dice Zhou. “Pueden cambiar de la palanca de alta recompensa a la de baja alrededor del punto de valor igual, mientras que en los animales con la mutación, el cambio ocurre mucho después. Su toma de decisiones adaptativa es mucho más lenta en comparación con los animales de tipo salvaje.”
Un circuito afectado
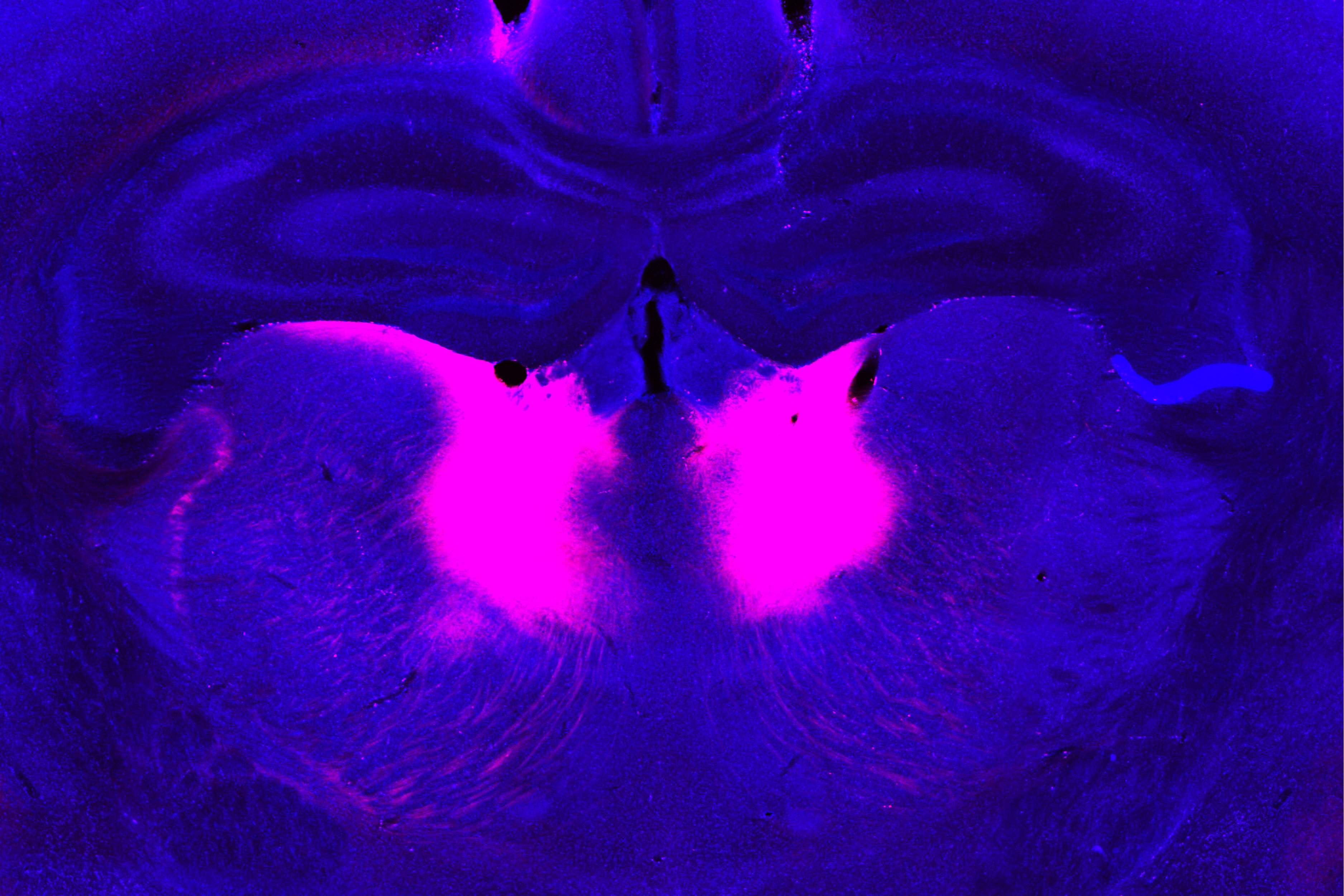
Mediante imágenes funcionales por ultrasonido y registros eléctricos, los investigadores encontraron que la región cerebral más afectada por la mutación grin2a era el tálamo mediodorsal. Esta parte del cerebro se conecta con la corteza prefrontal para formar un circuito talamocortical responsable de regular funciones cognitivas como el control ejecutivo y la toma de decisiones.
Los investigadores descubrieron que la actividad neuronal en el tálamo mediodorsal parece seguir los cambios en el valor de las dos opciones de recompensa. Además, los ratones mostraron diferentes patrones de actividad neural dependiendo del estado en que se encontraban: ya sea en estado exploratorio o comprometidos con un lado.
Los científicos también demostraron que podían usar optogenética para revertir los síntomas conductuales de los ratones con la mutación en grin2a. Modificaron las neuronas del tálamo mediodorsal para que pudieran ser activadas por luz, y cuando estas neuronas se activaban, los ratones empezaban a comportarse de manera similar a los ratones sin la mutación.
Aunque solo un pequeño porcentaje de pacientes con esquizofrenia tiene mutaciones en el gen grin2a, es posible que esta disfunción del circuito sea un mecanismo convergente del deterioro cognitivo para un subconjunto de pacientes con esquizofrenia con diferentes causas.
Dirigirse a este circuito podría ofrecer una forma de superar algunos de los deterioros cognitivos observados en personas con esquizofrenia, dicen los investigadores. Para ello, ahora están trabajando en identificar objetivos dentro del circuito que puedan ser potencialmente tratados con fármacos.
La investigación fue financiada por los Institutos Nacionales de Salud Mental, el Centro Poitras para la Investigación en Trastornos Psiquiátricos del MIT, el Colectivo Yang Tan del MIT, el Centro K. Lisa Yang y Hock E. Tan para Terapéuticas Moleculares en el MIT, el Fondo de Investigación Familiar Stelling en el MIT, el Centro Stanley para la Investigación Psiquiátrica, y la Fundación para la Investigación Cerebral y del Comportamiento.

MIT
Promover la investigación, las innovaciones, la enseñanza y los eventos y las personas de interés periodístico del MIT a la comunidad del campus, los medios de comunicación y el público en general, Comunicar anuncios del Instituto, Publicar noticias de la comunidad para profesores, estudiantes, personal y ex alumnos del MIT. Proporcionar servicios de medios a los miembros de la comunidad, incluido el asesoramiento sobre cómo trabajar con periodistas, Responder a consultas de los medios y solicitudes de entrevistas...